2026-02-09
2026年2月5日,刘河生教授团队主导的突破性研究成果登顶全球顶级科学期刊《自然》(https://www.nature.com/articles/s41586-025-10059-1),首次揭示并重新定义了帕金森病的核心病变环路——“躯体认知环路”,为帕金森病个体化无创治疗提供了全新靶点与路径。这项研究不仅是对帕金森病理机制的一次颠覆性重塑,更为我们正在推进的“个体化精准脑调控”提供了最坚实的科学基石。
作为“个体脑功能剖分(pBFS)技术”及帕金森病SCAN- Parkinson’s (SPARK)环路刺激治疗的独家转化方,银河脑科学致力于推动脑科学成果走向临床。我们希望通过这篇论文完整解读,帮助更多临床工作者、科研同仁及患者家庭,理解这项成果背后蕴含的治疗范式变革,这既是科学精神的延续,也是银河脑科学推动“精准脑环路刺激治疗”走向临床的初心。

研究背景:
帕金森病(PD)是一种以全身性运动及认知功能障碍为特征的神经退行性疾病。长期以来,传统观点将其局限于大脑特定局部运动区域的受损,但临床医生和患者都知道,事情没那么简单。
帕金森患者往往在这个“运动病”之外,还饱受非运动症状的折磨:严重的焦虑抑郁、顽固的失眠、莫名其妙的疼痛和自主神经功能紊乱。传统的“局部运动受损论”,就像盲人摸象,解释不了这些全身性的复杂症状。
如果帕金森病不仅仅是“动不了”,而是大脑的“指挥网络”出了问题呢?
随着脑科学的突破,研究者愈发认识到,大脑功能障碍往往是网络层面的全局问题。在此背景下,位于初级运动皮层内、与经典运动效应区(手、足、口)交错分布的“躯体认知动作网络”(SCAN)成为了新焦点。其功能横跨了动作执行、躯干运动、大脑唤醒及自主神经调控等多个维度,该网络功能紊乱极可能是导致PD多样化临床表现的核心机制。因此,探究其在PD中的病理特异性、现有临床干预(如药物、深部脑刺激(DBS)、经颅磁刺激(TMS))对该网络的调控机制,以及其作为未来精准神经调控新靶点的潜力,构成了本研究的核心探索方向。
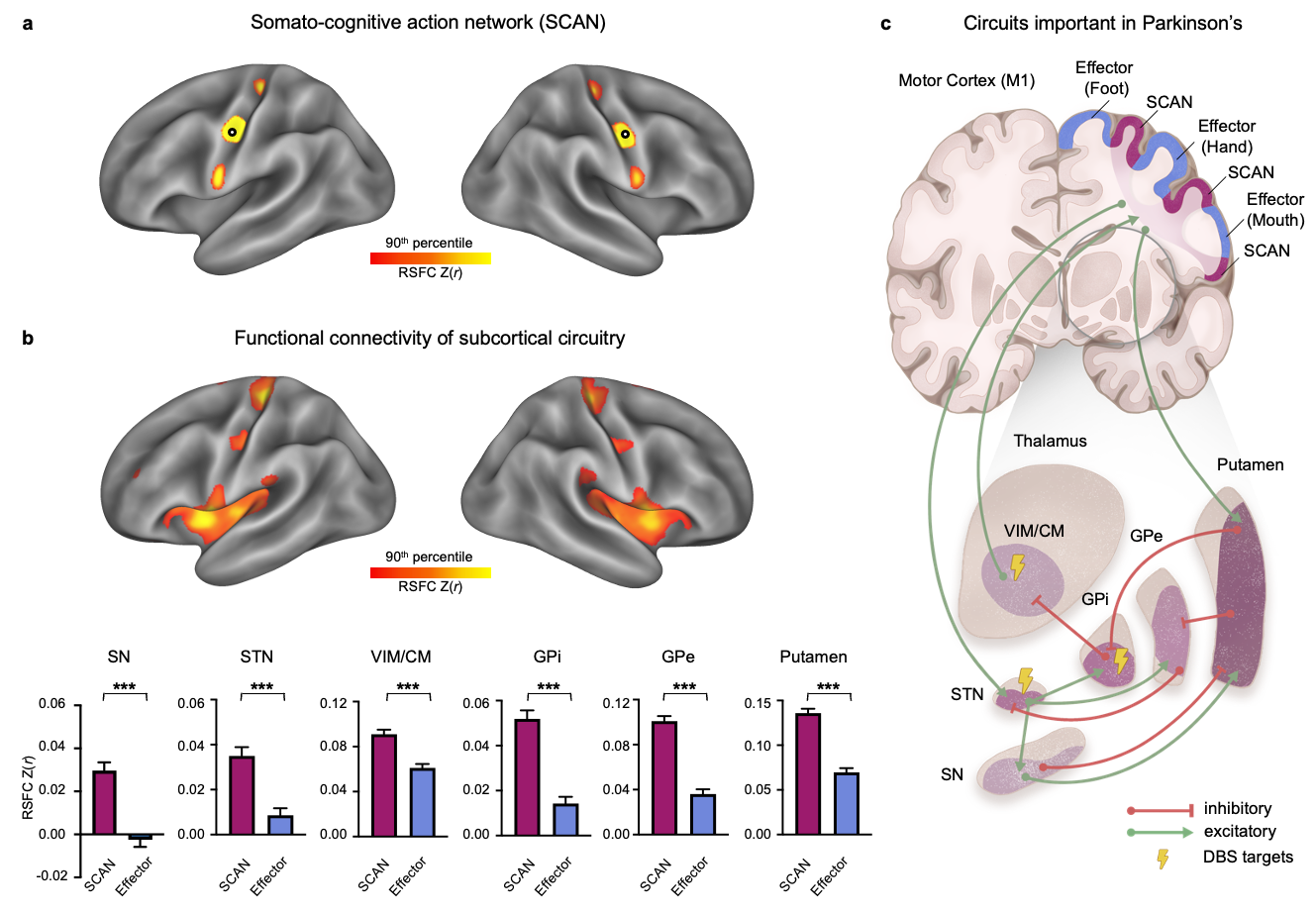
图1 PD相关皮层下核团与SCAN的特异性功能连接
(a)PD患者中SCAN与运动效应区交错的网络模式;(b)六个皮层下核团与SCAN的连接强度均显著高于与运动效应区的连接;(c)SCAN在PD环路中的位置及其与运动效应区的关系示意图
论文概要:
这篇发布于《自然》题为:Parkinson’s disease as a somato-cognitive action network disorder 的研究论文,由刘河生教授、任建勋、王聃红及河南省人民医院王梅云教授共同通讯发表(任建勋、张维为论文共同第一作者)。团队基于863人多模态临床影像数据集,抽丝剥茧,系统证实了PD的核心病理网络为SCAN网络。它为临床治疗带来了三个关键性“实锤”:
第一,抓住了“元凶”。研究发现PD患者存在SCAN网络与皮层下结构(黑质、丘脑底核等)的特异性功能连接过度增强,且这一现象为PD所特有,在其他运动障碍(如特发性震颤、肌张力障碍、肌萎缩侧索硬化)中未出现。
第二,揭示了“共性”。有效治疗(左旋多巴类药物、DBS、TMS、聚焦超声)均能降低这种过度连接。该研究为理解PD及开发精准环路刺激治疗提供了新方向。
第三,定义了“未来”。数据显示,相较于传统的“运动区”盲打,针对个体化SCAN靶点进行无创刺激治疗,疗效显著提升。这为未来从“局部试错”迈向“精准环路干预”提供了直接证据。
结果阐述:
研究整合了11个独立数据集,共863名受试者,包括PD患者、健康对照及其他运动障碍患者。采用静息态功能连接(RSFC)分析、皮层电生理记录(ECoG)、深部脑刺激(DBS)诱发响应、个体化功能剖分定位(pBFS)等技术,从多个维度探究SCAN在PD中的角色及其在治疗中的变化。
01 PD核心深部核团均与SCAN特异性连接
通过种子点RSFC分析发现,既往PD病理机制分析中已识别的六个关键皮层下核团(黑质SN、丘脑底核STN、丘脑腹中间核VIM/CM、苍白球内侧部GPi、苍白球外侧部GPe、壳核putamen),均体现出与SCAN环路的功能连接显著强于与运动效应区(脚、手、口)的功能连接(图1)。这提示PD相关的皮层-基底节-丘脑环路本质上是与SCAN连接的环路(SCAN-Parkinson’s (SPARK)环路),而非单纯的运动网络。
02 SCAN皮层下过度连接是PD的特异性病理机制
与健康对照组相比,PD患者在SCAN与上述六个皮层下核团之间的RSFC显著增强(图2)。这种过度连接具有特异性:在其他运动障碍(特发性震颤、肌张力障碍、肌萎缩侧索硬化症)中未出现,且仅发生在帕金森病患者中。此外,SCAN- Parkinson’s (SPARK)环路过度连接的程度与运动症状、认知功能、焦虑抑郁评分具有显著相关性,提示其临床意义。
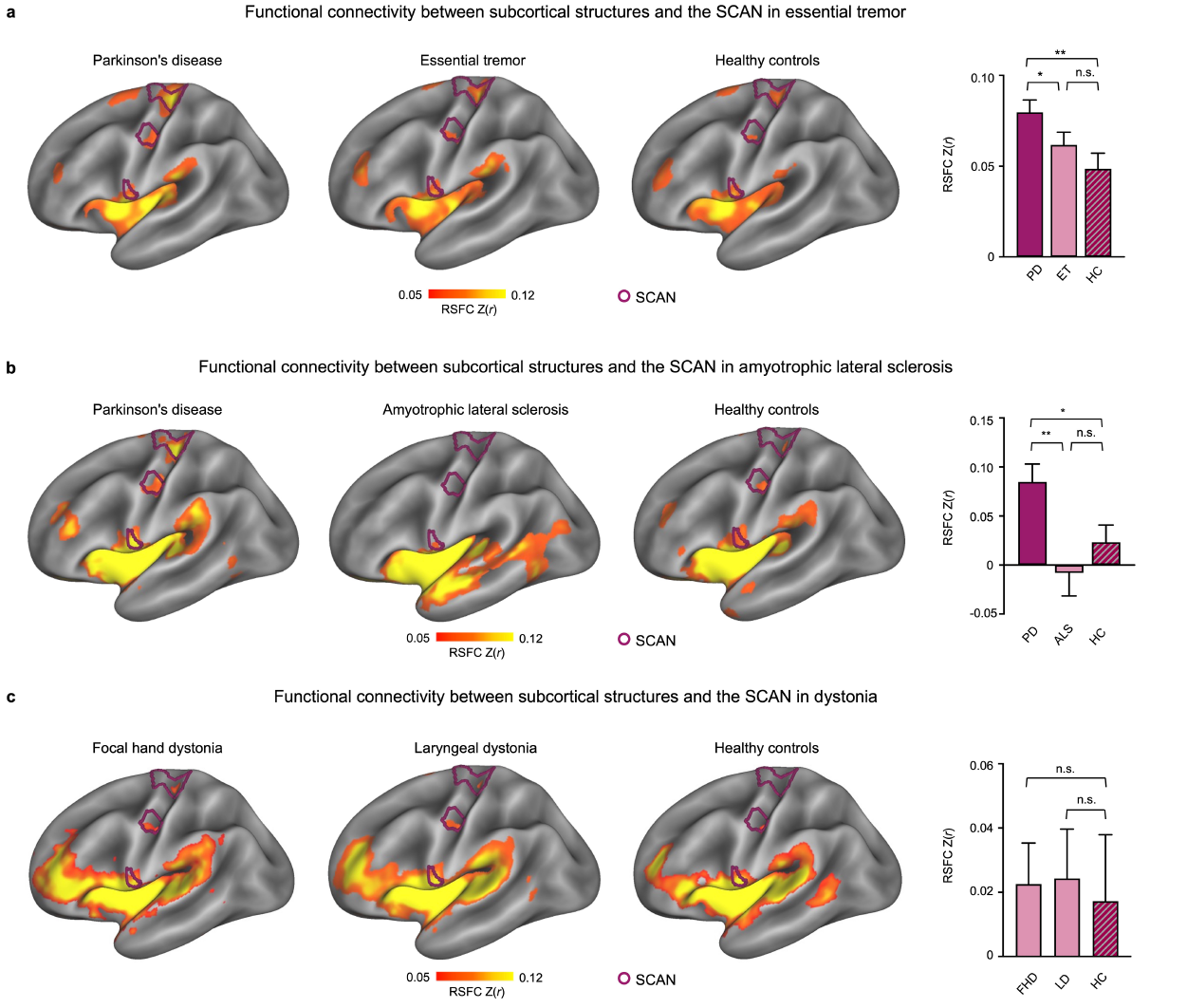
图2 SCAN- Parkinson’s (SPARK)-皮层下过度连接的组间比较
(a)左:PD患者静息态功能连接图;中:特发性震颤静息态功能连接图;右:健康对照静息态功能连接图;(b)左:PD患者静息态功能连接图;中:肌萎缩侧索硬化症静息态功能连接图;右:健康对照静息态功能连接图;(c)左:手部肌张力障碍静息态功能连接图;中:喉部肌张力障碍静息态功能连接图;右:健康对照静息态功能连接图;右侧均为连接强度柱状图
03 从现象到本源:SCAN- Parkinson ’s(SPARK)环路揭示PD多种治疗手段的共同起效机制
研究发现,DBS手术无论是STN、GPi还是VIM靶点,其有效的刺激区域均与SCAN的功能连接最强,显著高于与效应器区域的功能连接(图3)。ECoG记录进一步证实,当刺激STN时,在大脑皮层记录到的反应最强的电极主要集中于SCAN- Parkinson’s (SPARK)区域,其比例显著高于传统的运动效应区(图4)。这表明DBS本质上是通过调控SCAN- Parkinson’s (SPARK)环路发挥治疗作用。
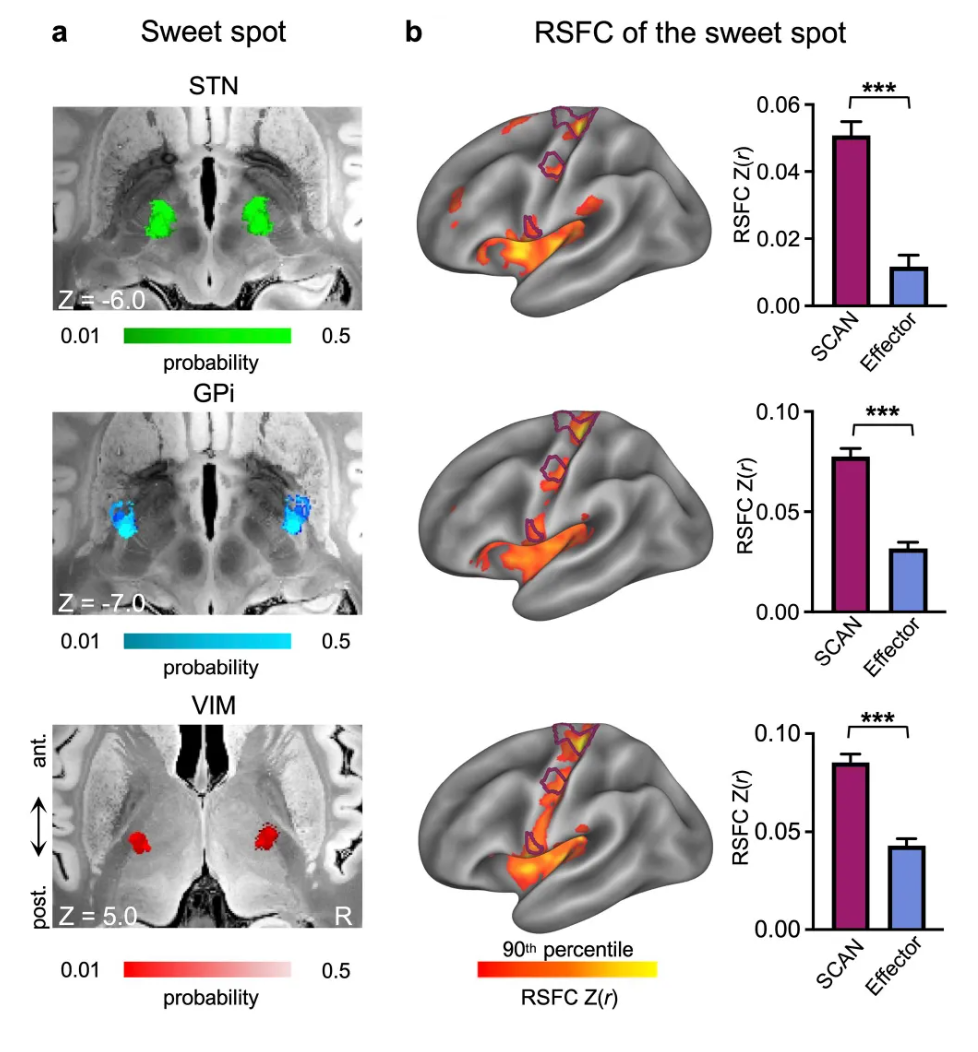
图3 有效DBS靶点的功能连接均集中于SCAN
(a)DBS“甜区”图谱:PD常用DBS靶点的“甜区”概率图,即最常带来显著疗效的刺激区域,包括:丘脑底核(STN,绿色)、苍白球内侧部(GPi,蓝色)和丘脑腹中间核(VIM,红色);(b)DBS“甜区”与SCAN网络的特异性连接:DBS各靶点与SCAN网络的功能连接强度均极显著地高于其与脚、手、口等运动效应区的连接强度
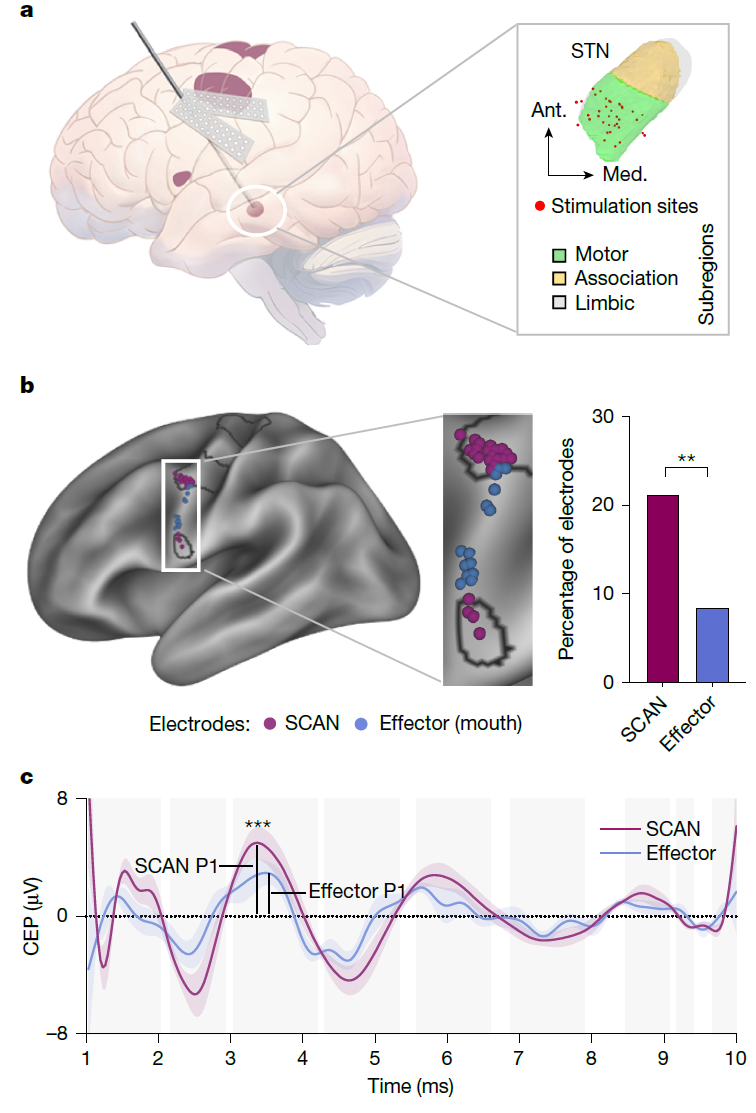
图4 深部脑刺激(DBS)在SCAN网络中诱发的皮层响应
(a)实验设计与电极布局;(b)响应电极分布:将刺激后反应最强的15%ECoG电极(即“响应电极”)投射到大脑皮层表面。紫色圆点代表SCAN区域电极,蓝色圆点代表位于运动效应区电极;(c)SCAN网络与运动网络的平均皮层诱发电位曲线。在刺激后10毫秒的时间窗口内,SCAN电极的振幅显著强于运动区网络电极(灰色阴影区域表示具有统计学差异的时间段)
纵向随访显示,STN-DBS术后患者SCAN与PD相关皮层下核团(SCAN- Parkinson ’s(SPARK))的过度连接逐渐降低,且连接降低程度与UPDRS-III评分改善显著相关(图5)。
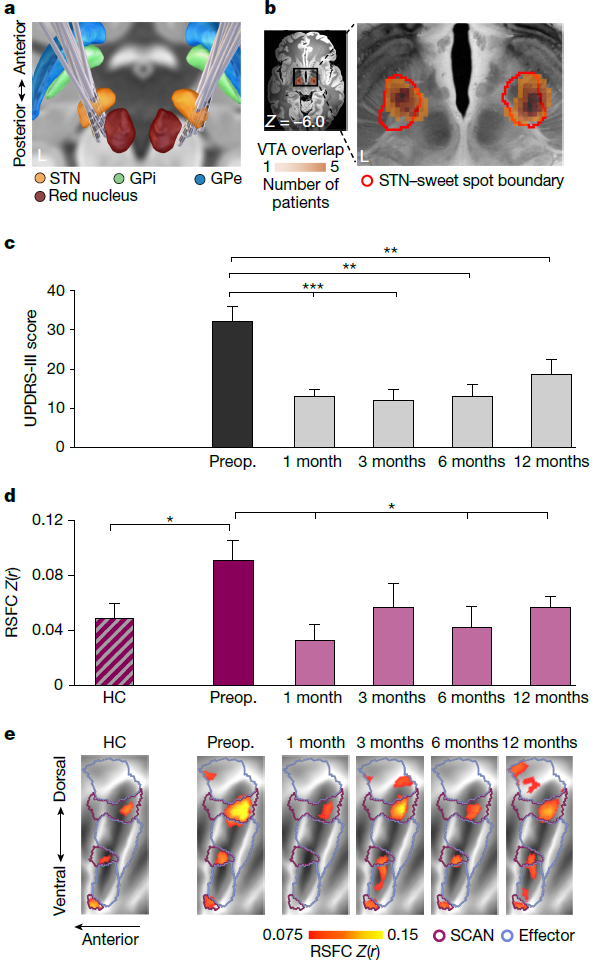
图5 STN-DBS对帕金森病SCAN- Parkinson ’s(SPARK)环路过度连接的影响
(a)DBS电极与刺激范围;(b)刺激靶点验证;(c)STN-DBS手术前后(基线及术后1、3、6、12个月)患者的运动症状评分(MDS-UPDRS-III)显著改善;(d)治疗前后SCAN与皮层下核团之间的功能环路(SCAN- Parkinson ’s(SPARK))连接强度变化:治疗前PD患者(紫色柱)的SCAN- Parkinson ’s(SPARK)环路连接强度显著高于健康对照(HC,条纹柱);治疗后DBS术后(粉色柱),过度连接在1、6、12个月时均出现显著下降;(e)皮层连接模式的可视化
在左旋多巴药物治疗中,用药后PD的运动症状显著改善,且SCAN- Parkinson’s (SPARK)环路过度连接显著下降(图6)。
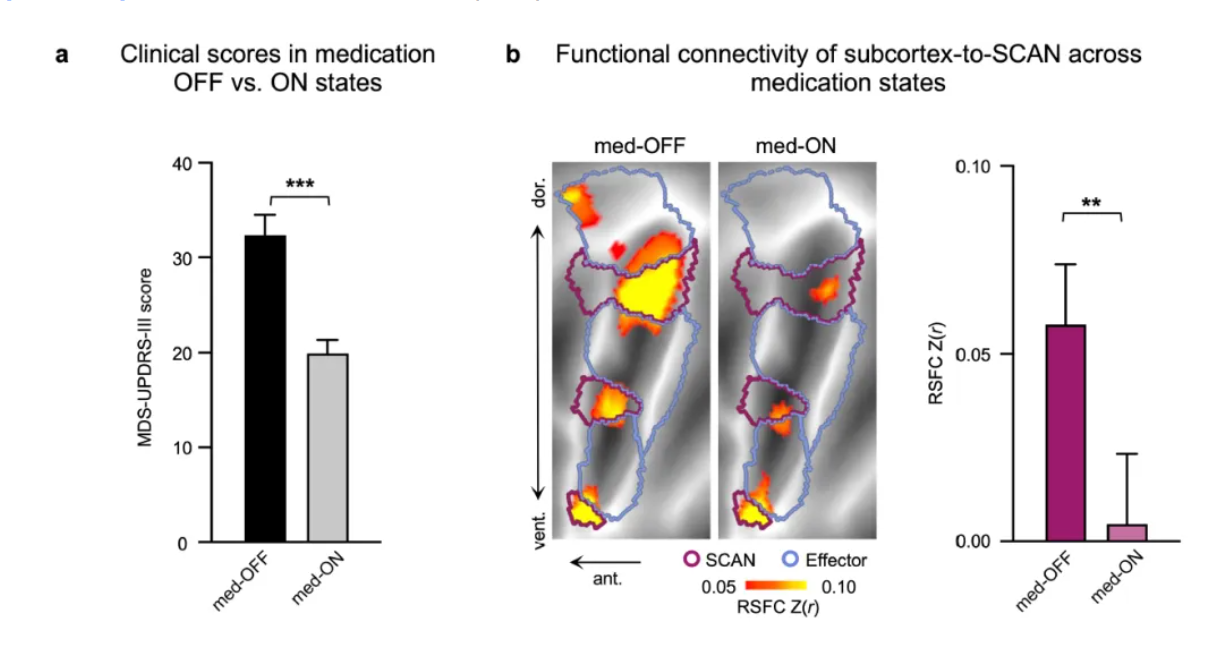
图6 多巴胺能药物可改善SCAN- Parkinson ’s(SPARK)过度连接
(a)临床症状的改善:患者服用左旋多巴后,其运动症状(MDS-UPDRS-III)得到显著的改善;(b)直接对比服药前(OFF)与服药后(ON)状态,SCAN-PD相关皮层下核团(SCAN- Parkinson ’s(SPARK))功能连接强度在用药后显著降低
丘脑磁共振引导聚焦超声(MRgFUS)VIM靶点越接近SCAN在丘脑中的功能“热点”,PD患者运动症状改善越明显(图7)。
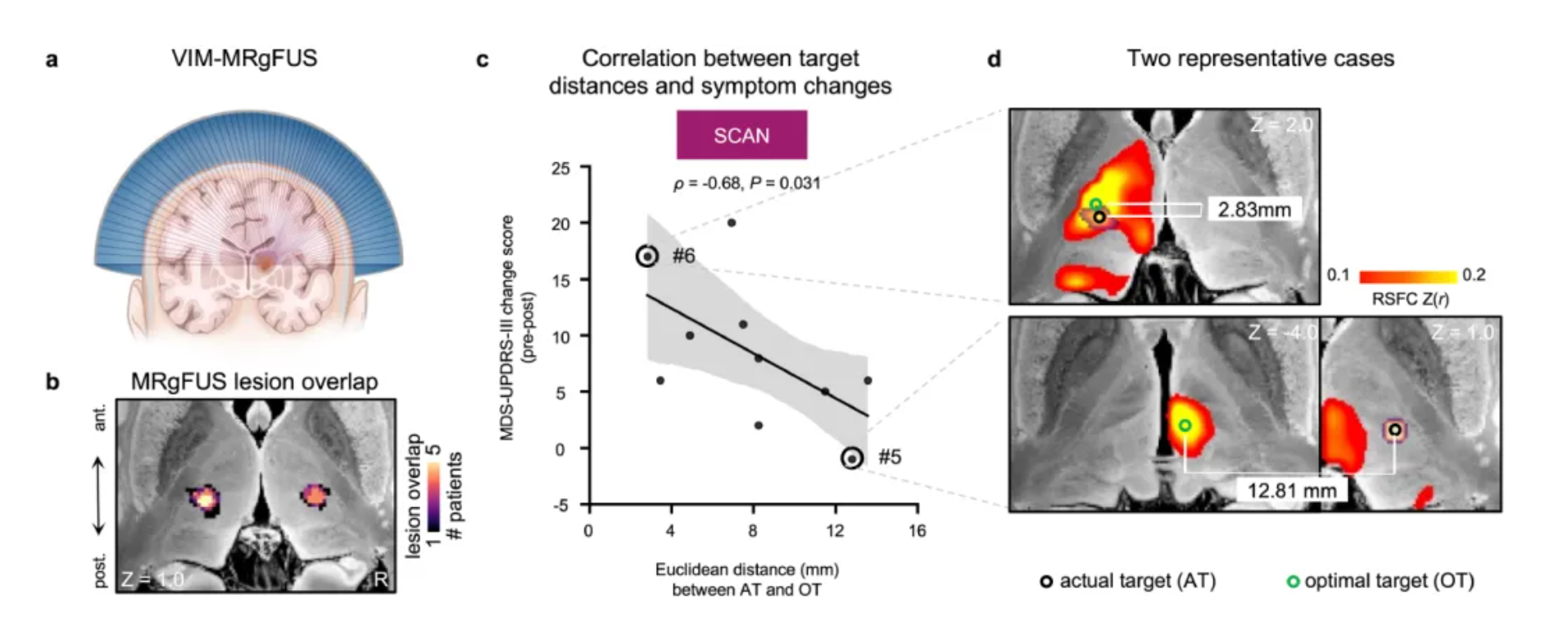
图7 聚焦超声靶点距SCAN“热点”越近,临床疗效越好
(a)治疗原理示意图;(b)患者毁损灶的重叠图谱;(c)个体化靶点与疗效的关系:实际毁损灶的位置离个体自身的SCAN功能“热点”越近,患者的临床症状改善就越明显。(d)典型案例对比:患者#6:实际靶点(黑圈)与SCAN最优靶点(绿圈)距离很近(2.83 mm),其临床改善非常显著(评分改善17分);患者#5:两个靶点距离很远(12.81mm),其临床改善微乎其微(评分改善-1分)
在此基础上,研究团队进一步检验了直接靶向SCAN的非侵入性神经调控(TMS)策略。在一项随机、盲法设计的临床试验中,36例帕金森病患者分别接受靶向SCAN或靶向传统运动区的TMS治疗。结果显示,两组患者症状均有所改善,但靶向SCAN组的症状缓解更快、幅度更大,在两周内的疗效约为传统运动区靶点的两倍。且靶向个体SCAN的TMS能够显著降低皮层SCAN—PD相关皮层下核团(SCAN- Parkinson ’s(SPARK) 环路)的过度连接(图8)。
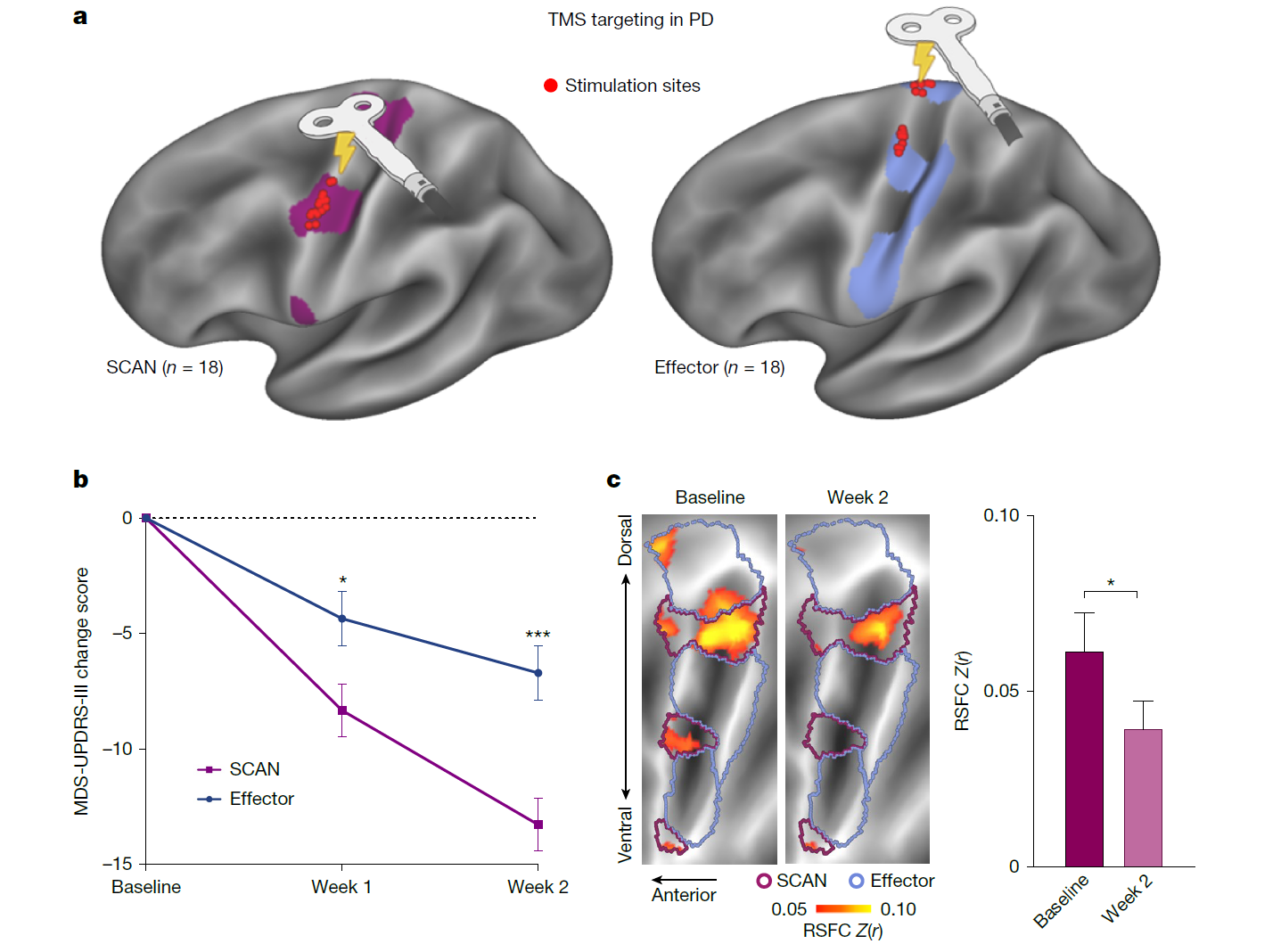
图8 靶向个体SCAN的TMS治疗优于个体运动效应区
(a)个体化SCAN与运动效应区靶点示意图;(b)SCAN组在2周个体化TMS治疗后MDS-UPDRS-III评分下降更显著;(c)治疗后SCAN- Parkinson ’s(SPARK)环路过度连接降低
结论与展望
本研究通过大样本数据,综合多模态影像、电生理、药物与神经调控证据,系统证实:PD的核心病理并非单纯的运动区损伤,而是以SCAN为核心的SCAN- Parkinson ’s(SPARK) 环路功能障碍。这一发现首次为药物治疗、深部脑刺激、无创脑刺激等多种PD疗法提供了统一的环路机制解释框架(图9)。
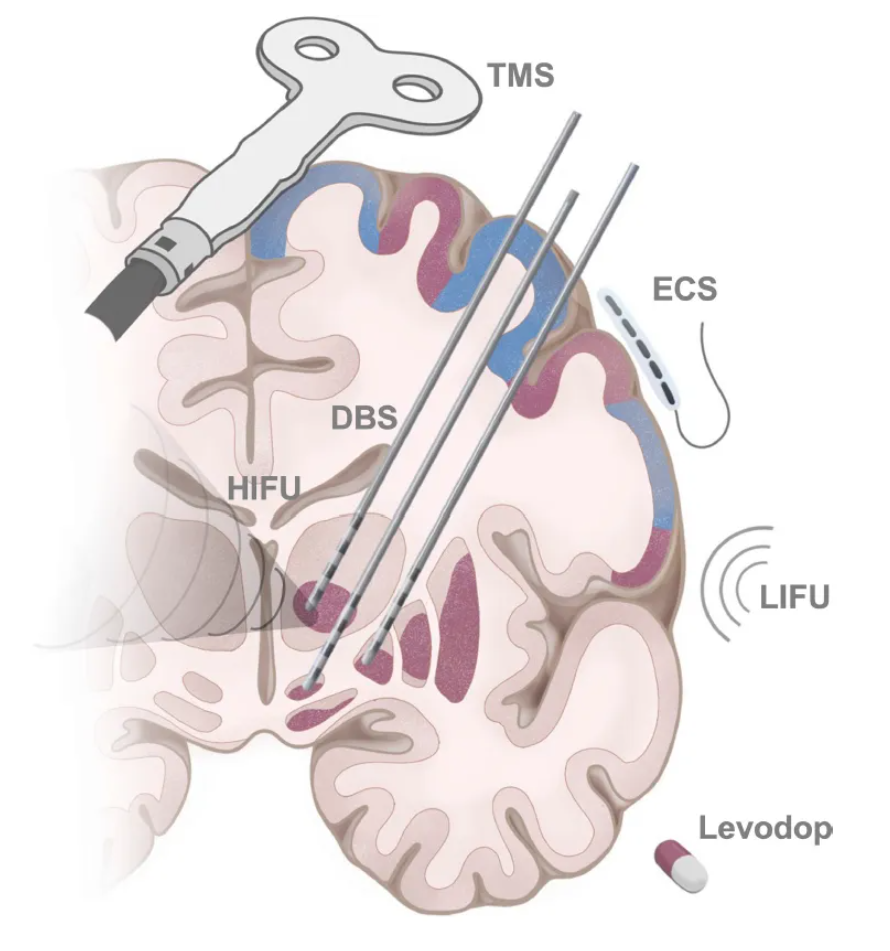
图9 PD多种治疗手段均作用于SCAN- Parkinson’s (SPARK)
其核心贡献在于:
提出新的病理模型:SCAN-PD相关皮层下核团(SCAN- Parkinson’s (SPARK))的过度功能连接是PD区别于其他运动障碍的特异性网络标志,与临床症状广泛相关;
揭示治疗共同机制:不同治疗方式(药物、DBS、TMS、超声)均通过调节SCAN- Parkinson’s (SPARK)环路发挥疗效,为“脑网络疗法”提供了理论依据;
开辟治疗新靶点:个体化SCAN靶点为无创神经调控(如TMS等)提供了新方向。
未来PD的治疗将从“局部核团调控”转向“个体化脑网络调控”。结合个体化的脑功能剖分定位技术,未来的临床干预将有望实现更精准、自适应、症状特异性的调控,真正推动PD治疗向“精准神经环路医学”迈进。
